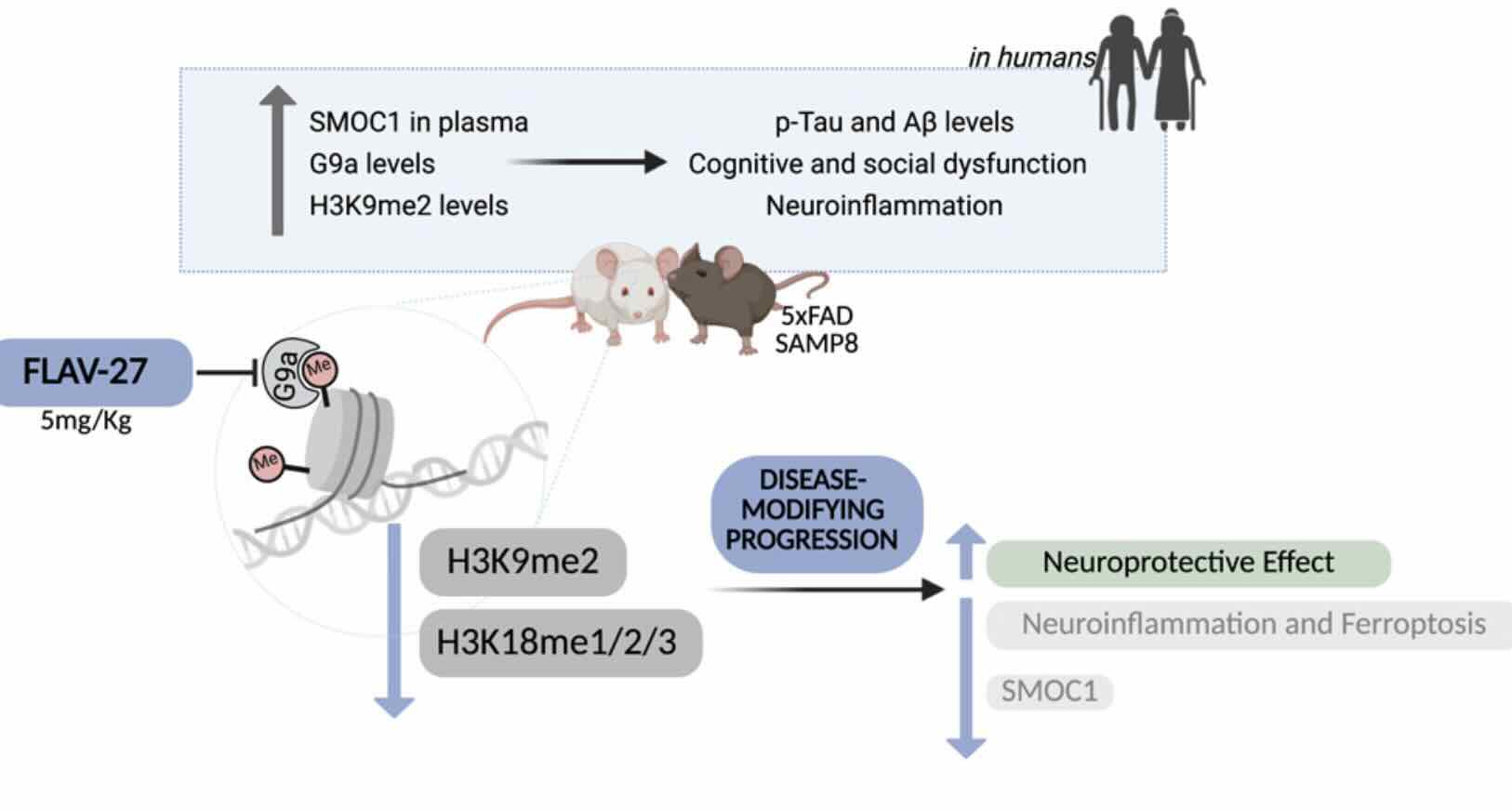
FLAV-27 verandert het epigenoom bij Alzheimerproefdiertjes de goede kant op (afb: Aina Bellver et al./Cell Molecular Therapy)
Onderzoekersters zouden een verbinding, FLAV-27 gedoopt, hebben ontdekt die het epigenoom (welk gen is actief en welk niet) zou herprogrammeren. Die behandeling zou in proeven met dieren die een vorm van Alzheimer hadden effectief zijn gebleken. Een volgende losse flodder in de eeuwigdurende zoektocht naar een effectief middel tegen Alzheimer of een methode die hout snijdt?
“De verbinding FLAV-27 vertegenwoordigt een innovatieve en veelbelovende benadering van de ziekte van Alzheimer, met het potentieel om het ziekteproces te beïnvloeden, omdat het niet alleen inwerkt op de symptomen of een enkele pathologische kenmerken, maar direct op de onderliggende moleculaire mechanismen”, zegt hoofdauteur Aina Bellver van de internationale universiteit van Catalonië (UIC) in Barcelona.
De ‘geneesmiddelen’ (ze genezen niet echt maar vertragen slechts de voortgang van de ziekte) die momenteel zijn goedgekeurd voor de behandeling van Alzheimer, zoals lecanemab en donanemab, zijn monoklonale antilichamen die werken door bèta-amyloïdeplaques uit de hersenen te verwijderen. “Hoewel ze een doorbraak betekenen, is hun effectiviteit beperkt, omdat ze de cognitieve achteruitgang slechts met 27% tot 35% vertragen, verschillende bijwerkingen hebben en alleen het deel van de pathologie aanpakken dat wordt veroorzaakt door de ophoping van bèta-amyloïde”, leggen de onderzoekersters uit.
FLAV-27 werkt daarentegen op een andere manier. Het is de eerste remmer in zijn klasse die het G9a-enzym beïnvloedt. Dit enzym is essentieel voor de epigenetische sturing van de hersens, omdat het helpt bij het uitschakelen van genen die fundamenteel zijn voor neuronale ontwikkeling, synaptische aanpasbaarheid (synaps is het contactpunt tussen hersencellen) en geheugenvastlegging.
Door G9a te remmen, voorkomt het nieuwe middel dat het natuurlijke molecuul S-adenosylmethionine (SAM) toegang krijgt tot het DNA. SAM is nodig voor de modificatie van DNA. Hierdoor wordt de epigenetische ontregeling, kenmerkend voor de ziekte van Alzheimer, vertraagd en kunnen neuronen hun normale functie herstellen.
De studie toont aan dat het remmen van G9a met FLAV-27 niet alleen klassieke pathologische kenmerken, zoals bèta-amyloïdeplaques en gefosforyleerde tau-eiwitten, die zich ophopen in de hersenen van mensen met de ziekte van Alzheimer, vermindert, maar ook de verstandelijke functies, het sociale gedrag en de structuur van neuronale synapsen herstelt in verschillende proefmodellen: in reageerbuistesten, de proeven in C. eleganswormpjes — waarin het de mobiliteit, levensverwachting en mitochondriale ademhaling verbetert — als ook proeven met muisjes met een vorm van Alzheimer in diverse stadia van voortgang.
Bewijs(?)
“In deze modellen is er bewijs van verbeterd kort- en langetermijngeheugen, ruimtelijk geheugen en sociale vaardigheden, wat niet alleen een effect op moleculaire markers aantoont, maar ook functioneel cognitief herstel,” stellen de onderzoekersters.
Volgens hen bevestigen deze resultaten dat epigenetische ontregeling niet slechts een bijwerking van de ziekte van Alzheimer is, maar een actief en beheersbaar mechanisme dat de belangrijkste kenmerken van de ziekte – zoals bèta-amyloïde-ophopingen, tauknopen, zenuwontsteking en synaptische disfunctie – verbindt via een gemeenschappelijke epigenetische veranderingen.
Een belangrijke bevinding die bijdraagt aan de waarde van deze behandeling is de vaststelling van een biomerker die zowel in de hersenen als in het bloedplasma van patiënten kan worden gemeten. De onderzoekersters ontdekten dat de epigenetische merker H3K9me2, het SMOC1-eiwit en het p-tau181-molecuul duidelijk verhoogd zijn en dat hun bloedspiegels direct te koppelen zijn aan symptomen zoals tauknopen, zenuwontsteking en de mate van verstandelijke stoornis. Wanneer FLAV-27 wordt toegediend aan proefdieren met een vorm van Alzheimer, keren deze indicatoren terug naar normale waarden, parallel aan het cognitieve herstel.
De beschikbaarheid van deze perifere bio-indicatoren is een van de belangrijkste aspecten die FLAV-27 onderscheidt van andere Alzheimergeneesmiddelen in ontwikkeling. “Het heeft belangrijke gevolgen voor toekomstige klinische studies, omdat het de selectie van geschikte patiënten mogelijk zal maken. Het middel kan worden getest met een eenvoudige bloedtest, door het effect van de behandeling te meten en aan te tonen dat het daadwerkelijk zijn therapeutische doelwit beïnvloedt,” stellen de auteurs.
Klinische proeven
Ondanks deze veelbelovende resultaten moet FLAV-27 nog verdere stappen doorlopen voordat klinische proeven bij mensen kunnen beginnen. Het middel bevindt zich momenteel in een vergevorderd preklinisch stadium. De volgende stappen zijn studies die veiligheid van deze methode bij ten minste twee diersoorten moeten vaststellen, om, na positieve resultaten uit te monden in de klinische proeven bij mensen. Dat kan alles bij elkaar nog jaren duren.
Deze nieuwe fase zal worden geleid door Flavii Therapeutics, een spruit van de UB, opgericht in 2025 en houder van de exclusieve licentie voor FLAV-27. Het bedrijf zal de preklinische en klinische ontwikkeling van het geneesmiddel op zich nemen, evenals het beheer van intellectuele eigendom en fondsenwerving, met als doel de kennis die aan de UB is gegenereerd om te zetten in nieuwe therapieën voor aandoeningen van het centrale zenuwstelsel, zoals de ziekte van Alzheimer.
Bron: Alpha Galileo
